功能團(tuán)的類型和離子交換中的持殊相互作用
同修 / 2022-07-04
功能團(tuán)的類型和離子交換中的持殊相互作用
最普通的強(qiáng)酸性陽離子交換劑的功能團(tuán)一SO3-,和最普通的強(qiáng)堿性陰離子交換劑的功能團(tuán)一CH2-N(R1R2R3) +表現(xiàn)出微弱的絡(luò)合物形成傾向;因此���,這些離子交換劑給出“正常”的親和力順序�,離子的電荷和水化程度決定了離子在這個順序中的位置�。對于含有其他功能團(tuán)的離子交換劑來說����,由于反離子與功能團(tuán)之間的相互作用會形成離子對或共價鍵����,情況通常要復(fù)雜得多��。這方面的一個例子是含伯胺�����、仲胺或叔胺基的陰離子交換劑對于OH-離子有很強(qiáng)的親和力�;同樣,酸型陽離子交換劑對于H+離子也有很強(qiáng)的親和力�����。這和強(qiáng)堿性陰離子交換劑或者強(qiáng)酸性陽離子交換劑形成鮮明的對照�,兩者分別把OH-離子和H+離子排在親和力順序的末端附近��。
羚酸型樹脂對于堿金屬的親和力順序是Li+>Na+>K+�,與磺酸型陽離子交換劑的親和力順序相反。帶羚酸功能團(tuán)的離子交換劑對于堿土金屬和某些過渡金屬也有強(qiáng)的親和力�����,這一點(diǎn)顯得與烷醇酸同這些金屬離子有生成難溶性鹽的傾向相一致。
膦酸樹脂對于 Th4+���、U4+�����、UO22+���、Fe3+、Pb2+�、Cu2+以及其他離子具有極強(qiáng)的親和力。
亞胺二醋酸樹脂對于過渡金屬離子和某些其他離子�,諸如Ag+, Hg2+, UO23+,VO2+,Pb2+,Th4+, Cu2+等有很高的選擇性�。
通過在樹脂的骨架結(jié)構(gòu)中引進(jìn)能與離子生成鰲合物的各種功能團(tuán)的方法,已經(jīng)合成出許多特殊的離子交換劑���。
一般地說����,給定離子與樹脂的功能團(tuán)所形成的離子對或絡(luò)合物越強(qiáng)�����,這種離子對于該離子交換劑的親和力就越大。有些現(xiàn)象可以用簡單的靜電模型解釋��。如同在6.4.2.2節(jié)中已經(jīng)提到的那樣����,所見堿金屬離子對于酸型離子交換劑的“逆轉(zhuǎn)”選擇性次序,可以解釋為:在高場強(qiáng)(rn小)的功能團(tuán)存在下��,式(6.22)中的第一項(xiàng)相對于反映水化度差異的第二項(xiàng)占了優(yōu)勢���。
TI+和Ag 離子與磺酸型離子交換劑之所以具有異乎尋常地高的親和力是由于這些離子有很強(qiáng)的極化能力�����。這就使得它們比較容易達(dá)到與功能團(tuán)最接近的距離�,此距離比根據(jù)離子半徑預(yù)期的還要短��。
離子與離子交換劑的化學(xué)作用有時可能導(dǎo)致驚人的效果�����。例如銅�、鉆����、鎳離子從中性鹽溶液中被弱堿性陰離子交換劑吸附���,以及Hg(Ⅱ)離子被磺酸型陽離子交換劑部分不可逆地吸著等。后一情況可能與生成有機(jī)汞化合物有關(guān)�。
在離子交換劑內(nèi)的特殊相互作用不必局限于固定在骨架上的功能團(tuán)。研究各種取代的季銨離子對于酚磺酸型陽離子交換劑的離子交換����,發(fā)現(xiàn)親和力順序是:NH4+<(CH3)4N+<(C2H5)4N+<(CH3)3AmN+<(CH3)2(C2H5)PhN+<(CH3)2PhBzN+。這個順序與考慮靜電作用力和可能的空間位阻效應(yīng)所預(yù)料的順序恰好相反����。在這種情況下,有機(jī)陽離子和樹脂的骨架之間可能存在著Van der Waals作用�����,隨著反離子中有機(jī)基團(tuán)的分子變大或芳香取代基的數(shù)目增多���,范德華引力也增大����。還必須提到,嫡效應(yīng)也是重要的�。有機(jī)離子有助于形成水的“冰山型”結(jié)構(gòu)(iceberg-typestructure),在這種結(jié)構(gòu)中�����,一個水分子以氫鍵與四個相鄰的水分子聯(lián)結(jié)�����。有機(jī)離子從水相進(jìn)入離子交換劑相時伴隨著體系嫡的增加���。還有數(shù)據(jù)表明����,某些金屬(Fe��, Ga, TI,Au,Sb)的鹵化物絡(luò)合物被磺酸型陽離子交換劑的吸著�,也可能是由于這些絡(luò)合物與樹脂骨架之間的化學(xué)作用所致。
交聯(lián)度
隨著交聯(lián)度的提高���,離子交換劑的溶脹程度減小����,含水量也隨之降低���。其結(jié)果是離子交換劑相的濃度增大���,這對于離子交換劑內(nèi)的特殊相互作用是有利的。隨著交聯(lián)度的提高����,溶脹壓力也升高了,根據(jù)Gregor的彈性骨架模型(見6.4.2.2節(jié))�����,這將會影響到離子交換劑對某些離子的親和力�����。因此��,隨著交聯(lián)度的提高��,這兩種影響將會提高離子交換劑的選擇性�����。實(shí)驗(yàn)中確實(shí)看到,對于普通的無機(jī)離子來說���,隨著交聯(lián)度的提高����,選擇性系數(shù)的確也升高了�,至少當(dāng)優(yōu)先離子(preferred ion)在離子交換劑中的當(dāng)量分?jǐn)?shù)相當(dāng)小時是這樣。
如果待交換離子很大����,則離子交換劑相中的“孔”可能太小而不允許離子自由地?cái)U(kuò)散到離子交換劑中去。其結(jié)果是離子被部分或完全地排斥在離子交換劑相之外�����。隨著交聯(lián)度的提高�,這種作用更加明顯。這類排斥作用被稱作“篩子作用”(sieveaction)����,它在無機(jī)離子交換劑中表現(xiàn)得最為突出。無機(jī)離子交換劑具有規(guī)則的���、相當(dāng)剛性的晶格和嚴(yán)格規(guī)定的孔徑���。在有機(jī)離子交換劑中����,由于樹脂骨架有柔性���,孔徑可以在一定限度內(nèi)變化。另外����,離子交換劑的不均勻性也會使孔徑有某種分布,而不是只有一種空徑��。
篩子作用可以導(dǎo)致選擇性的逆轉(zhuǎn)��。例如�����,對于交聯(lián)度較低的離子交換劑�����,四烷基銨離子表現(xiàn)出正常的親和力順序(NMe4<NEt4<NBu4)�����,但對于高交聯(lián)度的離子交換劑這種順序?qū)孓D(zhuǎn)。
對于痕量離子來說�,相對于主要離子的選擇性系數(shù)和分離因子通常都隨著交聯(lián)度的提高而增大。
一般地說���,待分離離子的水化度相差越大���,痕量離子的分離因子提高得越多。
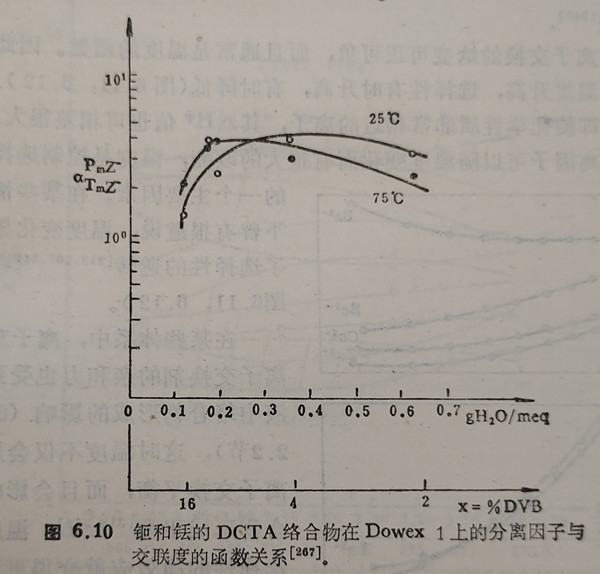
在分離大的離子�����,例如稀土元素的乙二胺四乙酸(EDTA)或反式-1�����、2-二般環(huán)已烷四乙酸(DCTA)絡(luò)合物時����,在選擇性系數(shù)對交聯(lián)度(有時也可以是分離因子對交聯(lián)度)的關(guān)系圖上發(fā)現(xiàn)有極大值。極大值的位置隨溫度而改變(圖6.10)����。在高交聯(lián)度的樹脂中���,大離子選擇性系數(shù)的降低是與這些離子被篩子作用排斥在離子交換劑相外有關(guān)的。













































![硫酸亞鐵銨標(biāo)準(zhǔn)溶液c[(NH4)2Fe(SO4)2]廠家價格](images/202207/thumb_img/1630_thumb_G_1658535105210.jpg)